L'ENCRE INVISIBLE
Les encres invisibles (ou encres sympathiques) ne deviennent visibles qu'avec un réactif chimique, de la chaleur ou une lumière ultraviolette. Voici une recette d'encre invisible utilisée en 1947 et la méthode pour la révéler.
1 Préparation
-Dissoudre une pointe de spatule de phénolphtaléine dans de l'éthanol , ou bien utiliser une solution déjà préparée de cet indicateur coloré.
-Dessiner au pinceau ou écrire avec un stylo à plume sur du papier.
2 Révélation
-Placer de l'ammoniaque (à 5% c'est suffisant) dans un cristallisoir, le tout dans un carton auquel on aura fait une fente sur le dessus.
-Introduire le papier par la fente et le tenir 5 minutes, le temps que les vapeurs d'ammoniaque (ammoniac ) réagissent.
3 Explications
-La phénolphtaléïne (III) est une molécule issue de la condensation de l'anhydride phtalique (I) et de deux molécules de phénol (II).
-Les substances nous apparaissent colorées quand elles absorbent de la lumière dans un domaine visible, c'est à dire le domaine de longueurs d'onde compris entre 400 et 800nm. La longueur d'onde de la lumière absorbée augmente lorsque le nombre de doubles liaisons conjuguées consécutives augmente. Pour qu'une molécule organique soit colorée, il faut qu'elle possède un nombre suffisamment grand (au moins 7) de doubles liaisons conjuguées consécutives.
-La phénolphtaléine est un colorant organique qui existe sous deux formes (deux molécules différentes) selon le Ph de la solution dans laquelle on le trouve. En solution, la forme (1) est incolore et la forme (2) est rose.
-La phénolphtaléine est incolore en milieu acide ou neutre. Un acide est une espèce chimique qui, en solution aqueuse, peut céder un ou plusieurs protons ( ion hydrogène H+).
-L'ammoniac est un gaz alcalin, basique qui va faire virer au rose l'indicateur coloré. Par opposition à un acide une base est une espèce chimique qui peut, en solution aqueuse, capter un ou plusieurs proton.
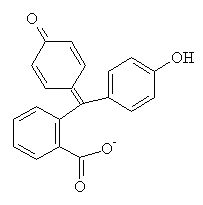
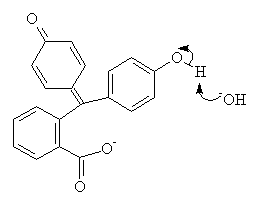
-En milieu acide, un proton d'un des groupes phénol est attaqué par un OH-. Il s'en suit une cascade de délocalisation électronique qui amène à la formation d'un ion carboxylate sur la forme basique de la phénolphtaléïne (2).
-Cette nouvelle molécule possède la propriété d'avoir son carbone central sous forme trigonale, c'est à dire lié à une double liaison. On voit que toutes les doubles liaisons de la molécule sont alors conjuguées. On a une telle délocalisation que la molécule devient colorée.
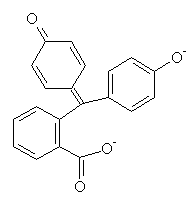
-Ainsi sous sa forme acide (1), la phénolphtaléine, avec quatre liaisons délocalisées est incolore tandis que sous sa forme basique (2), avec onze doubles liaisons conjuguées, elle absorbe dans le visible (vert-bleu) et apparaît de couleur rouge (rose en solution dilué). L’encre invisible connut ses dernières heures au début de la guerre froide, comme système d’appoint, peu à peu remplacée par les messages codés...
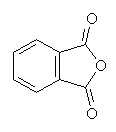
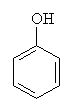
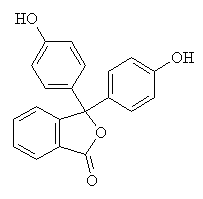

(I) Anhydride phtalique + 2 (II) Phénol = (III) Phénolphtaléine
(III) Phénolphtaléïne, forme acide (1) + OH-
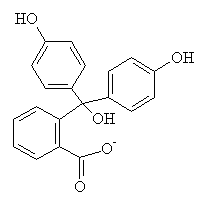
(IV) Phénolphtaléine, forme basique (2) + (-OH)
(IV) Forme basique de la phénolphtaléïne (2)